Zrozumieć zapłodnienie u roślin kwiatowych
Autorzy artykułu:
Edyta Ziegert*, Joanna Rojek
Uniwersytet Gdański, Wydział Biologii, Katedra Cytologii i Embriologii Roślin
*edyta0712(a)wp.pl
Mechanizm podwójnego zapłodnienia u Arabidopsis
Arabidopsis thaliana (rzodkiewnik, rodzina kapustowate; Fig.1) jest modelową rośliną, ze względu na swój niewielki genom (114.5 Mb/125 Mb całkowity; https://www.arabidopsis.org) oraz typ rozmnażania. Dzikie ekotypy rzodkiewnika występują prawie na całym świecie (FNA). A. thaliana charakteryzuje się niewielkimi rozmiarami (25-40 cm), krótkim cyklem życiowym (około 6 tygodni), samopylnością oraz licznie wytwarzanym potomstwem w postaci nasion. Wymaga zapłodnienia komórki jajowej i centralnej do prawidłowego rozwoju nasion.
Dzięki współczesnym technikom cytologicznym, ultrastrukturalnym oraz molekularnym, proces podwójnego zapłodnienia u Arabidopsis można śledzić na żywo, określać geny kontrolujące zapłodnienie oraz uzupełniać bądź weryfikować dotychczasowe poglądy (Hamamrura i in., 2012). W procesie podwójnego zapłodnienia u Arabidopsis można wyróżnić kilka etapów. W pierwszym etapie, dwie komórki plemnikowe, wraz z jądrem wegetatywnym łagiewki (lub bez), przedostają się do wnętrza gametofitu żeńskiego w rejon aparatu jajowego, a dokładnie do jednej z synergid. Degeneracja synergidy rozpoczyna się w wyniku bezpośredniego kontaktu z łagiewką pyłkową, ale tuż przed uwolnieniem jej zawartości do wnętrza gametofitu (Sandaklie-Nikolova i in., 2007). Jako, że plemniki są komórkami nieruchliwymi, pozbawionymi wici, sugeruje się, że uwolnienie zawartości łagiewki pyłkowej dokonuje się wyłącznie poprzez mechaniczny wyrzut komórek plemnikowych wraz z jądrem wegetatywnym w rejon aparatu jajowego (Hamamura i in., 2012). Po zdeponowaniu zawartości łagiewki, dwie komórki plemnikowe zostają przez krótki czas w fazie spoczynku wewnątrz gametofitu żeńskiego, pozostając w bliskim sąsiedztwie komórek docelowych: komórki centralnej i jajowej. W następnym etapie dochodzi do fuzji gamet: zachodzi plazmogamia (połączenie cytoplazmy), transport jąder plemnikowych przy udziale cytoszkieletu w kierunku jąder docelowych i kariogamia (połączenie jąder) komórek docelowych (Kawashima i in., 2014) (Fig. 2). Fuzja jąder docelowych zachodzi nieco wcześniej w komórce centralnej niż w komórce jajowej. W wyniku podwójnego zapłodnienia powstaje diploidalny zarodek oraz triploidalne bielmo. Bielmo będzie spełniało rolę odżywczą dla rozwijającego się zarodka (Faure i in., 2004).
U Arabidopsis nie stwierdzono preferencyjności w zapłodnieniu, co oznacza, że każda z dwóch komórek plemnikowych może zapłodnić komórkę jajową lub komórkę centralną z taką samą częstotliwością (Hamamura i in., 2012).
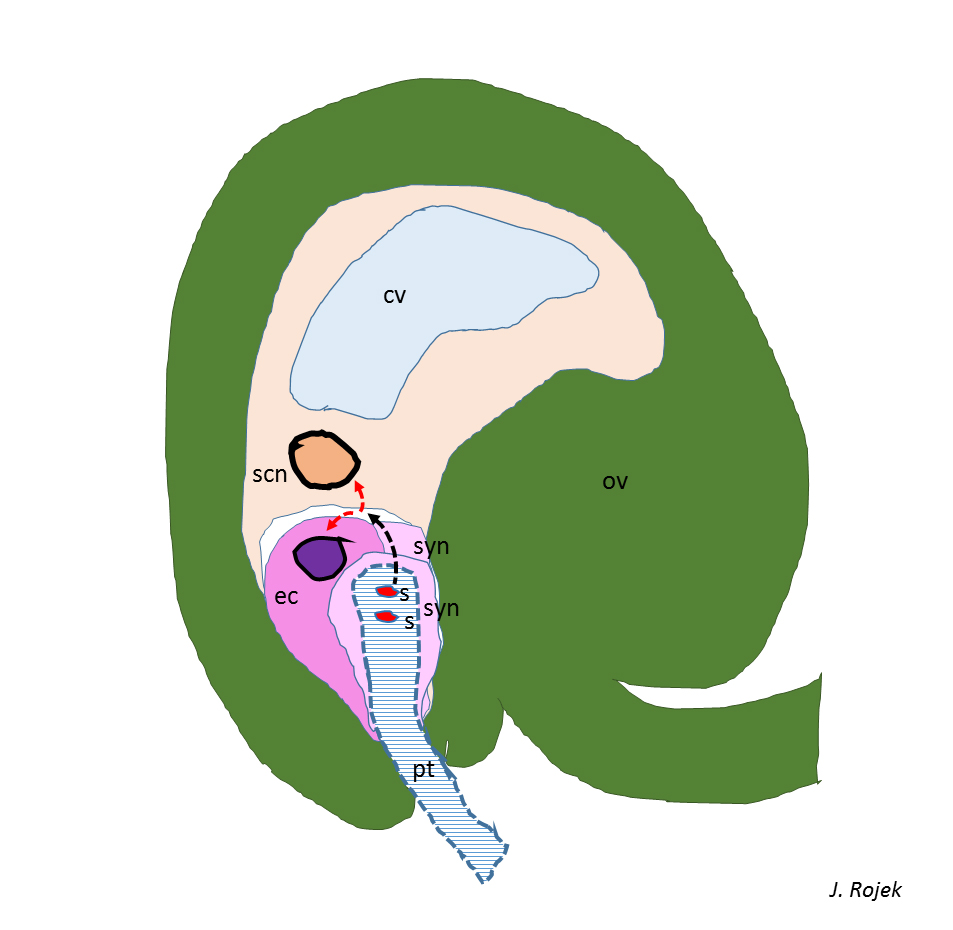
Fig. 2. Schemat podwójnego zapłodnienia u Arabidopsis. W pierwszym etapie, dwie komórki plemnikowe (s), dostarczane są do gametofitu żeńskiego dzięki łagiewce pyłkowej (pt), uwalniającej swoją zawartość w jednej z synergid (syn). Plemniki zostają biernie wyrzucone (czarna strzałka) do niewielkiej przestrzeni pomiędzy aparatem jajowym a komórką centralną i po fazie spoczynku i mobilizacji łączą się z komórkami docelowymi (czerwone strzałki). Pozostałe oznaczenia: zalążek (ov); komórka jajowa (ec); jądro wtórne komórki centralnej (scn); wakuola (cv). Autor – Joanna Rojek
Literatura:
Faure J. E., Rotman N., Fortune P., Dumas C., 2002. Fertilization in Arabidopsis thaliana wild type: Developmental stages and time course, The Plant Journal, 30(4):481-488
Hamamura Y., Nagahara S., Higashiyama T., 2012. Double fertilization on the move, Current Opinion in Plant Biology, 15:70-77
Kawashima T., Maruyama D., Shagirov M., Hamamura Y., Yelagandula R., Toyama Y., Berger F., 2014. Dynamic F-actin movement is essential for fertilization in Arabidopsis thaliana, eLife;3:e04501. DOI: 10.7554/eLife.04501
Rodkiewicz B., 1973. Eksperymentalna embriologia roślin, PWN
Sandaklie-Nikolova L., Palanivelu R., King E.J., Copenhaver G.P., Drews G.N., 2007. Synergid Cell Death in Arabidopsis Is Triggered following Direct Interaction with the Pollen Tube, Plant Physiology 4: 1753-1762
FNA, Flora of North America. Arabidopsis thaliana. Vol. 7 Page 226, 448, 450; http://www.efloras.org/florataxon.aspx?flora_id=1&taxon_id=200009201