Reakcja haloformowa
UWAGA: tekst został opracowany w oparciu o doświadczenia wykonane w Centrum Badań Molekularnych i Makromolekularnych PAN. Artykuł został opublikowany także w numerze 6/2020 czaspisma „Chemia w szkole”.

Po próbie Trommera prześwietlimy kolejną reakcję omawianą w szkole czy na studiach. Wiemy już, że wokół tej pierwszej próby krąży wiele nieprawdziwych i wręcz niedorzecznych opinii, ale o czy próba haloformowa jest w podobnym stopniu nasycona nieprawdziwymi i irracjonalnymi wręcz informacjami? Za moment się przekonamy!
Jak się uczymy, reakcja haloformowa, to reakcja w której otrzymujemy charakterystyczny żółty osad jodoformu CHI3, lub emulsję bromoformu CHBr3 o słodkawym zapachu czy też emulsję chloroformu CHCl3 – też o słodkim zapachu. Wszystkie te związki tworzą grupę haloformów (bo halogeny to z greckiego nazwa fluorowców, gr. halos – sól, słony, gdyż fluorowce znajdziemy w soli kamiennej, gdzie poza NaCl stanowiącym ponad 90% masy mamy jeszcze domieszki bromków i jodków i niewielkie ilości fluorków – w ilościach zależnych od złoża, np wydobywana na Podbeskidziu w postaci solanki sól zabłocka jest prawdopodobnie najbogatszym na świecie źródłem bromków i jodków). Z greki sól kamienną nazywamy halitem.
Reakcji tej ulegają metyloketony oraz metyloalkohole, czyli związki o wzorze ogólnym:
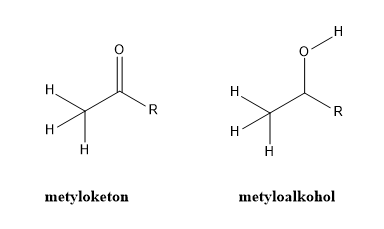
Gdzie R oznacza grupę alkilową lub arylową lub atom wodoru. Jeśli więc podstawnikiem będzie atom wodoru, to naszym „metyloketonen” będzie etanal, a metyloalkoholem – etanol.
Na naszym kanale YT można obejrzeć doświadczalny przebieg próby klikając tutaj.
Nieco historii
W 1822 roku George-Simon Serullas dodał kawałek metalicznego potasu do wodno-alkoholowego roztworu jodu (w czystej wodzie jod jest bardzo słabo rozpuszczalny, ale dobrze rozpuszcza się w etanolu, a więc im wyższe stężenie alkoholu w mieszanie woda-etanol, tym lepsza rozpuszczalność jodu). Wg innej wersji to kryształek jodu wpadł do wodno-alkoholowego roztworu KOH. Ku jego zdumieniu w probówce powstał żółty osad, oraz roztwór mrówczanu potasu. Osad, który był wtedy nieznanym chemikom związkiem został nazwany przed odkrywcę wodorojodkiem węgla. Zatem to etanol był pierwszym metyloalkoholem, dla którego odkryto tę reakcję. Reakcja przeprowadzona przez Serullasa jest jedną z pierwszych poznanych reakcji „organicznych”. Poniżej widzimy fragment oryginalnej publikacji Serullasa:

9 lat później w Stanach Zjednoczonych Samuel Guthrie w reakcji proszku bielącego, czyli proszku zawierającego m.i. chloran(I) wapnia (podchloryn wapnia) Ca(ClO)2 z etanolem otrzymał związek, który określił jako „zanieczyszczony eter chlorowy”. Niemal równocześnie ten sam związek pod nazwą „eter dwuchlorowy” otrzymał francuski naukowiec Eugene Soubeiran również w reakcji podchlorynu, ale nie wapnia a sodu z alkoholem. W tym samym roku także Justus Liebig potraktował chloral – produkt chlorowania etanolu zasadą i także otrzymał ten sam związek. Jednym słowem – działo się, bo niemal równocześnie ten sam związek odkryło 3 chemików w różnych częściach świata. Ja na ich miejscu zagrałbym jeszcze w lotka, tylko wtedy go pewno jeszcze nie było. A świat poznał nowy związek, który szybko zyskał zastosowanie do znieczulania podczas zabiegów chirurgicznych. Do Justusa Liebiga jeszcze powrócimy w dalszej części artykułu.
Krótko potem, bo w roku 1834 Jean-Baptiste Dumas w reakcji alkoholu z bromianem(I) sodu otrzymał kolejny związek, który wkrótce został przez niego nazwany bromoformem. Był też pierwszym, który określił skład związków otrzymanych przez Serullasa – CHI3, Guthrie, Soubeirana i Liebiga – CHCl3 oraz przez siebie – CHBr3. Wszystkie te związki w zasadowym środowisku ulegały hydrolizie do mrówczanów. On też nadał im nazwy: jodoform, chloroform i bromoform, nawiązując do produktu ich hydrolizy: łac. formica – mrówka.
Zatem reakcję wykonaną przez Serullasa możemy opisać równaniem:
![]()
A reakcję wykonaną przez Guthrie:

Przez Soubeirana:
![]()
Przez Dumasa:

Oraz przez Liebiga:
![]()
Wkrótce nadeszła fala licznych publikacji, których autorzy donosili, że otrzymali chloroform lub jodoform w reakcjach proszku bielącego lub jodu w zasadowym środowisku z wieloma związkami organicznych, m.i. metanolem oraz kwasem octowym czy octanem etylu.
Po raz pierwszy wiedzę tę usystematyzował Adolf Lieben w 1870 roku, który stwierdził, że:
„Pozytywny wynik próby jodoformowej dają związki zawierające grupę acetylową CH3CO połączoną z węglem lub wodorem, oraz związki, które w warunkach przeprowadzania próby zostają utlenione do takich, które zawierają tę jednostkę strukturalną.”
Udowodnił też, że doniesienia o próbie jodoformowej dla wielu związków są nieprawdziwe, a wynika to z obecności dużej ilości zanieczyszczeń w stosowanych odczynnikach, którymi często były aceton lub etanol. Po prostu w tamtych czasach trudno było o lepszej jakości odczynniki chemiczne, a dziś takowe nie miałyby racji bytu. Tak został wykluczony m.i. metanol z grona tych, które mają dawać haloform. Sama reakcja zaś została nazwana reakcją Liebena, choć jego nazwisko zazwyczaj jest pomijane przy nazwie reakcji. Wniosek Liebena został uogólniony także do innych halogenianów(I) (podhalogeninów).
Lieben pominął jednak związki, które praktycznie nie rozpuszczają się w warunkach zachodzenia reakcji i wnioski dotyczyły jedynie tych, które reagowały, bo były rozpuszczalne w rozpatrywanych warunkach. A co z pozostałymi metyloketonami i metyloalkoholami?
Tutaj na odpowiedź przyszło poczekać aż do roku 1934, kiedy to Reynold Fuson, Charles Tullock i Benton Bull opublikowali szereg wspólnych prac, w których zaproponowali inne warunki do przeprowadzenia próby – okazało się, że związki, których nie uwzględnił Lieben z powodu praktycznie braku rozpuszczalności, można rozpuścić najpierw w 1,4-dioksanie, a potem dodać wodnego r-ru zasady i jodu w jodku potasu. Wykazali w ten sposób słuszność wniosków Liebena także dla tych związków, dla których tamten nie mógł ich potwierdzić.
Jak przebiega reakcja? Mechanizm reakcji
Sposród wszystkich wspomnianych halogenów najszersze zastosowanie znalazła reakcja z jodem, zwana reakcją jodoformową. Wynika z praktycznych względów – łatwy w identyfikacji żółty osad o charakterystycznym zapachu. Przyjrzyjmy się cząsteczkowemu zapisowi tej reakcji dla metyloketonu:

W przypadku metyloalkoholu zużywa się więcej jodu:
![]()
Jest to oczywiście ogólny zapis sumaryczny. Jak wygląda ścieżka tej reakcji?
W środowisku zasadowym jod i inne halogeny ulegają przesuniętej w prawo dysproporcjonacji (dysproporcjonowaniu):

Oczywiście jon IO– jest w równowadze z HIO wskutek hydrolizy. Analogicznie z chloru otrzymuje się roztwór podchlorynu sodu, będący w istocie równomolową mieszaniną podchlorynu sodu i chlorku sodu z równowadze z niewielką ilością wolnego chloru, którego zapach czujemy po otwarciu pojemnika z roztworem podchlorynu, np. chlorowym wybielaczem. To właśnie jony IO–, ClO– lub BrO– oraz wolne halogeny i wolne kwasy halogenowe(I) HXO występujące w niewielkiej równowagowej ilości odpowiadają za zajście reakcji. Jony I–, Cl– czy Br– nie biorą udziału w reakcji. Jony halogenianowe(I) łatwo utleniają metyloalkohole do metyloketonów:
![]()
Oprócz przechodzenia halogenów we wspomniane jony i cząsteczki trzeba sobie zdawać sprawę, że ketony w obecności zasady ulegają enolizacji z wytworzeniem anionu enolanowego:

Jon enolanowy chętnie ulega reakcjom z elektrofilami. W literaturze można spotkać różne wersje mechanizmu: od wolnych chlorowców, przez kwasy halogenowe(I) do anionów halogenianowy(I). Tutaj zostanie on przedstawiony na cząsteczce kwasu jodowego(I) (podjodawego). Pamiętajmy, że atom chlorowca łączy się z silniej elektroujemnym tlenem, przez co ma on cząstkowy ładunek dodatni (δ+) – jest elektrofilem, chętnie więc ulegnie reakcji z donorem pary elektronowej. Wolna para elektronowa zgromadzona na węglu atakuje dodatnio naładowany atom chlorowca i tworzy się nowe wiązanie C-I. Jednocześnie umożliwia to przeskok wiążącej pary elektronowej I-O na tlen i odejście grupy OH–, co widzimy poniżej:
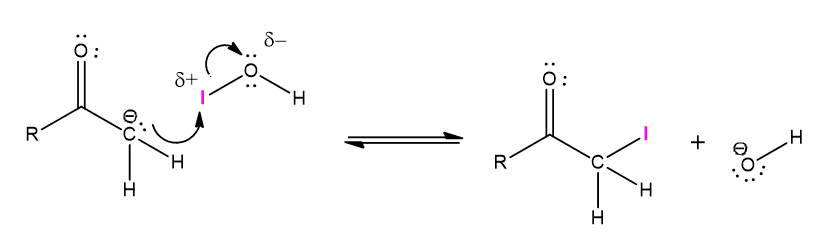
Następnie anion OH– powoduje odejście drugiego protonu:

I powtarza się etap z cząsteczką kwasu jodowego(I):

A potem proces powtarza się jeszcze raz:

W tym momencie otrzymaliśmy związek 1,1,1-trihalo-2-karbonylowy. Gdyby wyjściowym związkiem był acetaldehyd, to produktem byłby trijodoacetaldehyd. A w przypadku użycia roztworu podchlorynu sodu produktem byłby trichloroetanal, zwany zwyczajowo chloralem:

Zatrzymajmy się w tym miejscu – czy to nam już czegoś nie mówi? Czy to nie związek użyty przez Justusa Liebiga? Ależ oczywiście że tak! Justuś Liebig nieświadomie, ale dostarczył cennej informacji o ścieżce tej reakcji. Przeprowadził reakcję chloralu z zasadą i otrzymał chloroform, a chloral to przecież związek typu 1,1,1-trihalo-2-karbonylowego. Analogiczny związek powstaje w zasadowym środowisku próby haloformowej. Wspólnym mianownikiem jest tutaj zasada – to ona powoduje, że w reakcji powstaje haloform – węgiel karbonylowy staje się centrum elektrofilowym, posiada cząstkowy ładunek dodatni wskutek wyciągania elektronów przez tlen, jak i przez grupę CI3, CCl3 czy CBr3. Teraz z naszym związkiem w środowisku zasadowym dzieje się coś cudownego – ulega on reakcji z jonem OH-, ale już w inny sposób niż to przedtem było. Teraz celem ataku jest węgiel karbonylowy. Tworzenie nowego wiązania C-O powoduje, że węgiel ten przekracza swoją pojemność walencyjną – jedna z wiążących par elektronowych przeskakuje na węgiel tak powstaje kwas karboksylowy i anion trihalometylowy:

Lecz to jeszcze nie koniec: otrzymaliśmy obok siebie cząsteczkę kwasu (donora protonu) jak i anion trihalometylowy – zasadę tak silną, że jon OH- jest przy niej tam jakąś sobie słabą zasadą. Mamy kwas, mamy zasadę – co jeszcze musi się stać? Odszczepienie protonu od kwasu i przeniesienia bo na bardzo silną zasadę:

I tym oto sposobem dobrnęliśmy do końca – otrzymaliśmy haloform i anion karboksylowy. Produktami reakcji haloformowej są więc haloform i sól kwasu karboksylowego. Wbrew dość powszechnej opinii z podręczników szkolnych – w próbie haloformowej nie otrzymujemy kwasu karboksylowego!
Zanim przejdziemy dalej wyjaśnimy sobie coś. Metyloketony chętnie reagują z wolnym chlorowcem dając 1,1,1-trihalo-2-on lub trichloroetanal, gdy reakcji poddamy etanal – jedyny aldehyd spełniający warunki do zajścia tej reakcji. Reakcję da się zatrzymać na etapie tej pochodnej, o ile u układzie reakcyjnym nie ma zasady zdolnej do reakcji z karbonylowym atomem węgla, co powoduje rozpad wiązania C-C. Dlatego też przepuszczając chlor przez etanal (lub etanol, który jest najpierw utleniany przez chlor do etanalu) otrzymujemy chloral – związku tego jednak nie można wydzielić w próbie haloformowej ze względu na zasadowe środowisko – po prostu w obecności zasady jest tylko produktem pośrednim, który natychmiast przechodzi w ostateczny produkt: chloroform i anion mrówczanowy. Justus Liebig nieświadomie przeprowadził ostatni etap tej złożonej reakcji.
Często pomijaną rzeczą jest fakt, że poza haloformem w próbie tej można otrzymać także tetrahalometan – dotyczy to zwłaszcza sytuacji, gdy mamy zdecydowany nadmiar halogenianu(I) – haloform ulega następczej reakcji z nim, np:

Po prostu im większy nadmiar utleniacza, tym więcej haloformu przejdzie w tetrahalometan lub przejdzie cały, jeśli zostawić mieszaninę reakcyjną na odpowiedni czas.
Zapraszamy do obejrzenia wideo:
Podsumowując:
Przypadek kwasu octowego i octanów
Wokół kwasu octowego często są kontrowersje. Już na start powinniśmy sprostować, że reakcji tej właściwie musiałaby ulega sól tej kwasu, bo musimy ją przeprowadzić w zasadowym środowisku. Czy jednak kwas octowy da osad jodoformu? Wiele osób argumentuje: tak, bo posiada ugrupowanie CH3CO – to prawda, posiada. Ale nie jest metyloketonem – tu jednak ktoś zawoła: ale etanal też nie jest ulega! No i konflikt gotowy, czego dowodem są fora internetowe i grupy dyskusyjne na FB. A czy ktoś to sprawdził doświadczalnie?
Powróćmy teraz do faktów historycznych: przed badaniami Liebena donoszono o osadzie jodoformu przeprowadzając reakcję ze związkami wielu typów m.i. metanolu, kwasu octowego, octanu etylu. Metanol i część innych związków zostały wykluczone przez Liebena, który udowodnił, że wynik jest zafałszowany przez zanieczyszczenia, takie jak metanol czy aceton. Ostatecznie listę Liebena wyczyścili Furson, Tullock i Bull. Czy jednak tak było w przypadku kwasu octowego i octanu etylu? To zanieczyszczenia, czy sam kwas i ester? Za moment się przekonamy!
To, że zarówno etanal jak i kwas octowy/octan posiadają ugrupowanie acetylowe, nie oznacza że będą się tak samo zachowywać wobec tego samego substratu. Etanal posiada atom wodoru połączony z grupą acetylową, a kwas musi być najpierw przeprowadzony w sól, czyli jon octanowy. Tutaj sytuacja zmienia się diametralnie – w jonie octanowym mamy delokalizację ładunku ujemnego wskutek rezonansu, a węgiel karbonylowy nie posiada takiego ładunku dodatniego, jak w etanalu czy acetonie. Zarówno etanal jak i kwas octowy reagują z chlorem w podobny sposób:
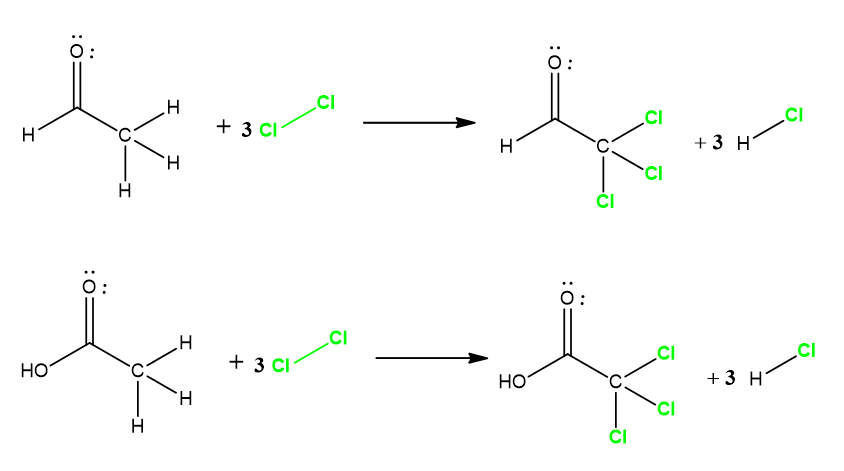
Jednakże produkty chlorowania zachowują się wobec zasady zgoła odmiennie:

Po prostu w drugim przypadku mamy do czynienia z reakcją zobojętniania. A co gdyby jednak kwas octowy (a właściwie jego sól ze względu na potrzebę zalkalizowania środowiska) ulegał próbie haloformowej, np. chloroformowej? Anion trichlorooctowy byłby produktem pośrednim i w środowisku zasadowym musiałby się rozpaść na chloroform i anion węglanowy:

W praktyce oznaczało by to, że sole kwasu trichlorooctowego w roztworze wodnym musiały by się rozpadać na węglany i chloroform. A tymczasem istnieję i mają się dobrze. Weźmy pod lupę jeszcze aceton – produktami reakcji haloformowej są haloform oraz anion octanowy – a przecież anion octanowy musiałby także ulegać tej próbie i reagować dalej! Gdyby kwas octowy ulegał reakcji, to aceton reagowałby zupełnie inaczej, co sumarycznie wyglądało by tak:

Aceton dawałby wiec 2 razy więcej cząsteczek haloformu, niż ilość wzięta do reakcji. Byłby więc bardzo wydajnym jego źródłem. Co ciekawe, to jest znana taka reakcja:

Jednakże produktami reakcji haloformowej dla acetonu są zawsze anion octanowy i haloform, co znaczy, że halogenowanie zachodzi tylko przy jednym atomie węgla, podczas gdy drugi nie bierze w tym udziału. Heksahaloaceton nie jest produktem pośrednim reakcji haloformowej, ani anion octanowy jej nie ulega, przez co z mola acetonu otrzymujemy tylko 1 mol haloformu.
Pamiętamy, że chlorowce wprowadzone do roztworu silnej zasady ulegają dysproporcjonowaniu do halogenku i halogenianu(I). Co jednak się stanie, gdy dodamy kwasu octowego do roztworu zawierającego tę mieszankę jonów, np. I– i IO–? Kwas jako że zakwasza środowisko cofa równowagę tej reakcji i wydziela się wolny jod:

Co widzimy poniżej:

Mamy więc potwierdzenie, że reakcji tej musiałyby ulegać tylko sole tego kwasu (lub środowisko reakcji musiałoby zawierać odpowiedni nadmiar zasady celem zobojętnienia kwasu). Podobnież też reakcji ten nie ulega octan etylu, który także jest obiektem wielu sprzeczek. Choć w niektórych szkolnych i pozaszkolnych opracowaniach można znaleźć informację, że kwas octowy ulega tej reakcji, to pamiętajmy, że nader często jest to efekt bujnej fantazji autorów, którzy nader często piszą o rzeczach, których nie widzieli, ale wydaje im się że powinno działać. Cóż, często tylko wydaje im się… Niech podsumowaniem wszystkiego będzie, że nie są znane wyjątki od reguły sformułowanej przez Liebena.
Reakcje analogiczne do próby haloformowej
Warto wspomnieć o reakcjach analogicznych do omawianej. Zastanówmy się, a gdyby tak zamiast wodorotlenku sodu czy potasu użyć innej zasady? Pierwszą modyfikacją niech będzie użycie amoniaku zamiast wodorotlenku. Co wtedy otrzymamy?

Tak więc otrzymaliśmy amid w analogicznej reakcji. A w przypadku, gdy zamiast wodnego ośrodka użyjemy alkoholu i alkoholanu jako zasady?

Jednakże ze względu na trudności w oderwaniu protonu od grupy alkilowej, anion Cl3C– pobiera proton od znacznie bardziej kwasowego alkoholu:

Sumaryczne równanie reakcji wygląda więc następująco:

Co tutaj dostrzegamy? Że zasada z substratu stała się katalizatorem reakcji! Wystarczy mała ilość alkoholanu i reakcja napędza się sama.
Na koniec przyjrzyjmy się reakcji, która pojawiła się także w ostatnim numerze czasopisma Antocyjan:
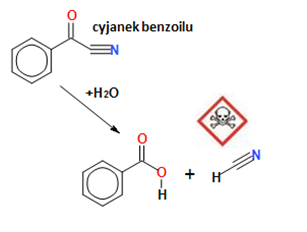
Czy widzimy w tym równaniu analogię do próby haloformowej? Jeśli tak, to się bardzo dobrze składa. Po prostu 3 atomy chlorowca zastąpiono jednym atomem azotu, za to trójwiązalnym. Jak widać w tym przypadku rolę zasady może pełnić woda, która przecież ma wolne pary elektronowe i także w niewielkim stopniu dysocjuje na jony OH–.
Podsumowanie
Wyjaśniliśmy sobie czym jest próba haloformowa i co jej ulega łącznie z kłopotliwymi przypadkami. Jak widać, jest ona otoczona mniejszą ilością herezji, niż opracowana wcześniej próba Trommera, a głównym przekłamaniem jest, że w reakcji tej powstają kwasy, a nie sole, lub to, że ulega jej kwas octowy.

Reakcja jodoformowa z metyloalkoholem – czy na pewno zgadzają się współczynniki? Po lewej 4 Na, a po prawej w sumie 6 🙂